- Занятие №2 «Адсорбция на подвижной границе раздела»
- Исходный уровень:
- Содержание занятия:
- Вопросы для самоподготовки:
- Практическая часть
- Вычислите площадь, занимаемую одной молекулой изоамилового спирта в поверхности раздела вода-воздух и длину молекулы, если Г∞ = 8,7·10-9 моль/м2 , М = 88, ρ = 0,8528·103 кг/м3 .
- Основные величины, используемые для характеристики поверхностных явлений, коллоидных систем, растворов ВМС
- 💥 Видео
Видео:Изоамиловый спирт, о дробной перегонке от канала НеОбзор58 ПензаСкачать

Занятие №2 «Адсорбция на подвижной границе раздела»
«Адсорбция на подвижной границе раздела»
Изучить сущность мономолекулярной адсорбции Ленгмюра на границе газ — раствор; газ — твердое тело; Изучить основные положения полимолекулярной адсорбции газов на твердых адсорбентах; Изучить уравнения Гиббса, Шишковского, Ленгмюра, Фрейндлиха, БЕТ и знать, что они характеризуют; Научиться строить изотерму поверхностного натяжения и определять графически поверхностную активность на основе опыта; Научиться рассчитывать поверхностную активность по уравнению Гиббса; Научиться объяснять характер различных изотерм адсорбции; Научиться решать графические задачи с использованием выше перечисленных уравнений.
Видео:Изоамиловый спирт, теория дробной перегонкиСкачать

Исходный уровень:
1. Повторить теоретические вопросы к занятию №1
Видео:Изоамиловый спирт, теория дробной перегонкиСкачать

Содержание занятия:
Видео:7.1. Спирты: Номенклатура, классификация, изомерия. ЕГЭ по химииСкачать

Вопросы для самоподготовки:
Практическая часть
Работа №1 «Изучение адсорбции ПАВ на границе раздела жидкий раствор-воздух»
Цель работы: 1. Изучение адсорбции на границе жидкий раствор ПАВ – воздух. 2. Построение изотермы поверхностного натяжения у = f (c). Определение поверхностной активности ПАВ и построение изотермы адсорбции Г = f (c).
Приборы и реактивы: 1. Сталагмометр. 2. Мерные колбы на 50 см3 – 8 шт. 3. Бюретка на 25 мл. 4. Водные растворы ПАВ. 5. Дистиллированная вода.
Из 2м раствора ПАВ путем последовательного разбавления дистиллированной водой готовят семь растворов ПАВ, следующих концентраций: 1,5м, 1м, 0,75м, 0,5м, 0,25м, 0,1м. Сталагмометрическим методом, измеряют поверхностное натяжение приготовленных растворов ПАВ. Результаты эксперимента заносят в таблицу и строят изотерму поверхностного натяжения у = f (c) при температуре опыта. По изотерме поверхностного натяжения на ходят величину поверхностной активности: g = — ( dу/dc) с→0 Графически находят значение (dуi/dci) и вычисляют величину избыточной адсорбции для каждой концентрации ПАВ. Значение Гiпомещают в таблицу. Строят изотерму адсорбции Гi = f (ci).
Поверхностное натяжение и избыточная адсорбция
Концентрация раствора, моль/л
Поверхностное натяжение, Дж/м2
Избыточная адсорбция, моль/м2
Форма отчета: необходимо построить изотерму поверхностного натяжения и изотерму адсорбции на миллиметровой бумаге и сделать вывод.
Вопросы для самоконтроля:
Что такое капиллярная конденсация. Ее физико-химическая сущность. Приведите примеры ПАВ. Как схематически обозначают эти молекулы?
1.Число капель раствора, вытекающего из сталагмометра при данной температуре, равно 111. Число капель воды в тех же условиях 57. Поверхностное натяжение воды равно 0,0733 н/м. Вычислить поверхностное натяжение раствора, если его плотность равна 888 кг/м3, плотность воды 1000 кг/м3.
2. Вычислите длину и площадь молекулы изоамилового спирта в насыщенном адсорбционном слое, если Г∞=7·10-10 моль/см2, М=63 г/моль,
При изменении поверхностного натяжения 0,1М раствора капроновой кислоты сталогмометром, число капель было 75, для воды – 25 капель, с=1; 
Примеры решения задач:
Рассчитать адсорбцию (моль/см2) масляной кислоты на разделе водный раствор – воздух при t=220С, если поверхностное натяжение воды при этой температуре 72,2·10-3Дж/м2, а 0,1М раствора масляной кислоты
Для расчета величины адсорбции на разделе раствор-газ используют уравнение Гиббса: 
у1= 72,2·10-3; у2= 62·10-3; у2 у1
Δσ=σ2- у1= 62·10-3 — 72,2·10-3= — 10,2·10-3;
Видео:ПОЛЕЗНАЯ ХИМИЯ: ИЗОПРОПИЛОВЫЙ СПИРТСкачать

Вычислите площадь, занимаемую одной молекулой изоамилового спирта в поверхности раздела вода-воздух и длину молекулы, если Г∞ = 8,7·10-9 моль/м2 , М = 88, ρ = 0,8528·103 кг/м3 .
| ? Заказ №: 22180 |
| ⟾ Тип работы: Задача |
| ? Предмет: Химия |
| ✅ Статус: Выполнен (Проверен преподавателем) |
| ? Цена: 153 руб. |
? Как получить работу? Ответ: Напишите мне в whatsapp и я вышлю вам форму оплаты, после оплаты вышлю решение.
➕ Как снизить цену? Ответ: Соберите как можно больше задач, чем больше тем дешевле, например от 10 задач цена снижается до 50 руб.
➕ Вы можете помочь с разными работами? Ответ: Да! Если вы не нашли готовую работу, я смогу вам помочь в срок 1-3 дня, присылайте работы в whatsapp и я их изучу и помогу вам.
⚡ Условие + 37% решения:
Вычислите площадь, занимаемую одной молекулой изоамилового спирта в поверхности раздела вода-воздух и длину молекулы, если Г∞ = 8,7·10-9 моль/м2 , М = 88, ρ = 0,8528·103 кг/м3 .
Решение: Максимальное число адсорбированных молекул на 1 м2 составляет Г∞·NА (NА – число Авогадро). Следовательно, площадь, занимаемая молекулой в насыщенном адсорбционном слое (площадь поперечного сечения молекулы), равна Г NА S 1 Толщина насыщенного адсорбционного слоя, то есть длина молекулы ПАВ вычисляют по формуле Г M l где: M молярная масса ПАВ, кг/кмоль; плотность ПАВ, кг/м3 .
Научись сам решать задачи изучив химию на этой странице:
|
Услуги:
|
Готовые задачи по химии которые сегодня купили:




















































Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
Видео:Урок 13 (осн). Взаимодействие молекул. Смачивание и несмачиваниеСкачать

Основные величины, используемые для характеристики поверхностных явлений, коллоидных систем, растворов ВМС
| Свободная поверхностная энергия | E = σ ∙S, Дж Е →min | Термодинамическая функция, характеризующая энергию межмолекулярного взаимодействия частиц на поверхности раздела фаз с частицами каждой из контактирующих фаз | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Абсолютная адсорбция (удельная) | А = 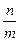 , моль/г , моль/г | Равновесное количество поглощаемого вещества, приходящееся на единицу поверхности раздела фаз или на единицу массы твердого адсорбента | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Относительная адсорбция на подвижной поверхности раздела фаз(уравнение Гиббса) | Г = 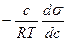 | Величина, аналогичная абсолютной адсорбции, отражает зависимость между поверхностной концентрацией адсорбируемого вещества и его концентрацией в объёме раствора | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Поверхностная активность | 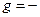 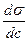 , Дж∙м/моль или Гиббс , Дж∙м/моль или Гиббс | Способность растворенных веществ изменять поверхностное натяжение растворителя | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Изотермы адсорбции | Г = Г 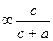 , (1) Г-величина адсорбции; Г , (1) Г-величина адсорбции; Г 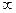 — предельная адсорбция; с- равновесная концентрация адсорбата; а -величина, обратная константе адсорбционного равновесия; Г = kc — предельная адсорбция; с- равновесная концентрация адсорбата; а -величина, обратная константе адсорбционного равновесия; Г = kc 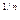 (2) если n>1, Г = kc n если n (2) если n>1, Г = kc n если nЗадача 1. Рассчитайте, пользуясь уравнением Фрейндлиха, сколько органической кислоты может быть поглощено почвой, если в почвенном растворе установилась равновесная концентрация 2,7ммоль/л. Константы уравнения Фрейндлиха равны: К=4,5, 1/n=0,4. Решение: уравнение Фрейндлиха Г=К×С 1/ n , подставим данные задачи: Г=4,5×С 0,4 . Прологарифмируем его : lgГ=lg4,5+0,4lgC. Подставим значение С и найдем lgГ по таблице логарифмов: По таблице антилогарифмов найдем: Г= 6,70 ммоль/100г Задания для индивидуальной самостоятельной работы 39. Поверхностное натяжение водного раствора поверхностно-активного вещества с концентрацией 0,056 моль/л при 293 К равно 4,33×10 -2 н/м. Вычислите адсорбцию этого вещества из раствора с концентрацией 0,028 моль/л. 40. Вычислите длину и площадь молекулы изоамилового спирта, если известна предельная адсорбция Г¥ = 7,0×10 -6 моль/м 2 (плотность изоамилового спирта равна 0,81 г/мл). 41. В раствор объемом 60 мл некоторого вещества с концентрацией 0,440моль/л поместили твердый адсорбент массой 3 г. После достижения адсорбционного равновесия концентрация вещества снизилась до 0,350 моль/л. Вычислите величину адсорбции. 42. По экспериментальным данным определите константы в уравнении Ленгмюра: Равновесная концентрация, моль/л: 88,7; 177,7; 260,0. Адсорбция, ммоль/г: 1,50; 2,08; 2,88. 43. Определите адсорбцию уксусной кислоты на животном угле при 25 0 С, если равновесная молярная концентрация кислоты равна: 0,062 моль/л и 0,882 моль/л. Константы: а = 0,155 моль/кг, 1/n = 0,42. 44. –52 .Что такое адсорбция? Какие виды адсорбции наблюдаются в почвах? Рассчитайте количество уксусной кислоты, адсорбированное 100 г почвы из раствора концентрации “С” (см.таблицу), если в уравнении Фрейндлиха К=9,5, 1/n=0,22.
Коллоидная химия Свойства коллоидных систем, их получение И очистка коллоидов Ответьте на вопросы: 1. Дайте определение коллоидной химии. Какие науки и где в практике используют ее достижения? 2. В чем проявляется количественное сходство и качественное различие между суспензиями, коллоидными и истинными растворами? 3. Дайте определение понятиям дисперсная система, дисперсная фаза, дисперсионная среда, степень дисперсности. 4. Дайте классификацию дисперсных систем по степени дисперсности, указав гомо- и гетерогенные системы. 5. В чем сходство и в чем различие растворов высокомолекулярных соединений и лиофобных коллоидов? 6. Дайте определение понятию коллоидный раствор, сравните свойства истинных и коллоидных растворов. 7. Кратко опишите основные методы получения коллоидных растворов. 8. Что такое диализ? Ультрафильтрация? 9. Опишите методы очистки коллоидных систем. Подчеркните свойства коллоидных систем, на которых основаны эти методы. Какую роль играет мембрана при диализе коллоидных систем? 10. Почему осмотическое давление коллоидных растворов значительно меньше истинных? 11. Опишите, как образуются коллоидные растворы при дроблении горных пород. Как связаны эти процессы с почвообразованием? 12. Какие оптические явления наблюдаются в коллоидных системах в отличие от истинных растворов? 13. Дайте объяснение эффекту Фарадея — Тиндаля. Как связано это явление с законом рассеяния света Рэлея? 14. В чем сущность закона рассеяния света Рэлея? Как на основе этого закона объясняется световые явления в коллоидных растворах? 15. Объясните сущность нефелометрии. Где применяются нефелометры? 16. Каковы причины существования двойного электрического слоя мицеллы? 17. Возможно ли по реакции двойного обмена образование золя, если исходные вещества взяты в эквивалентном количестве? 18. Что такое термодинамический и электрокинетический потенциал? 19. Какая связь между величиной дзета — потенциалом и устойчивостью коллоидных систем? 20. Назовите силы, действующие между коллоидными частицами. 21. Какие скачки потенциалов выделяют в мицелле? 22. Что такое электрофорез? Как связана величина дзета-потенциала со скоростью электрофореза? 23. Что такое электроосмос? От каких факторов зависит величина электроосмоса? 24. Назовите основные методы получения коллоидных систем. Какова роль стабилизатора? Задания с выбором ответа 25. Гетерогенная система, в которой дисперсионная среда является газом, дисперсная фаза – жидкостью, называется… а) гидрозоль; б) аэрозоль ; в) эмульсия; г) суспензия 26. В коллоидном растворе, полученном при взаимодействии силиката калия с избытком серной кислоты, потенциалопределяющим ионом является… 27. Как получают суспензии из истинных растворов? а) диспергированием; б) конденсацией; б) гранулированием; г) разложением 28. Сенсибилизация — это явление, которое… а) увеличивает агрегативную устойчивость системы; б) уменьшает агрегативную устойчивость системы в) не изменяет агрегативную устойчивость; г) сначала увеличивают агрегативную устойчивость, затем её уменьшают. 29. Для лиофобных дисперсных систем характерна а) гомогенность; б) гетерогенность; в) низкая степень раздробленности дисперсной фазы; г) термодинамическая устойчивость 30. Лиофильные системы характеризуются: а) самопроизвольным образованием б) термодинамической неустойчивостью; г) выраженной межфазной границей. 31. Какая формула мицеллы, соответствует раствору, полученному сливанием равных объемов электролитов 0,01н KCl и 0,001н AgNO3. 32. Способность дисперсной системы противостоять силе тяжести, называется кинетической или __________ устойчивостью. а) седиментационной; б) потенциальной; в) гетерогенной; г) характеристической 33. Метод седиментационного анализа на основе уравнения Стокса позволяет определить______ частиц дисперсной фазы. а) энергию частиц; б) размер; в) силу отталкивания; г) силу притяжения 34. Методы получения дисперсных систем, основанные на объединении более мелких частиц в более крупные, называются… а) конденсационными; б) пептизационными в) гидродинамическими; г) диспергированием 35. При освещении коллоидного раствора проходящим светом наибольшему рассеиванию подвергаются ___ волны а) короткие; б) все; в)длинные; г) средние 36. Количественной характеристикой дисперсных систем, которая используется для их классификации, является ____ частиц дисперсной фазы. а) масса; б) размер; в) форма; г) число 37. Ион, находящегося в избытке вещества обладающей сродством к ядру мицеллы и адсорбирующийся на его поверхности, называется… а) потенциалопределяющим; б) ядерным в) дисперсионным; г) коагулирующим 38. Потенциалопределяющим ионом в системе, образующейся согласно уравнению H2SO4(изб) + BaCl2 = BaSO4 + 2HCl, является a) Н + ; б) Ва 2+ ; в) SO4 2- ; г) Cl — 39. С помощью метода нефелометрии можно определить ______ коллоидной частицы а) размер; б) заряд; в) плотность; г) показатель преломления 40. В природе диспергирование веществ, сопровождающееся образованием дисперсных систем, происходит при … а) землетрясениях; б) фотосинтезе; в) вулканических извержениях; г) светорассеянии 41. Перемещение частиц дисперсной фазы под действием внешнего электрического поля называют… а) электрофорезом; б) электроосмосом; в) потенциал протекания; г) потенциал седиментации 42. Как называют явление, при котором окраска коллоидных растворов в рассеянном свете (при рассмотрении сбоку) и в проходящем свете неодинакова а) опалесценция; б) флуоресценция; в) седиментацией; г) коагуляцией Задания для индивидуальной самостоятельной работы 43. -52. Напишите формулы мицелл, полученных сливанием равных объемов электролитов указанной ниже концентрации. Приведите название всех слоев мицеллы. Укажите место возникновения дзета-потенциала.
53- 62. а) Что такое электрофорез? б) Как величина скорости электрофореза зависит от величины дзета-потенциала? в) По данным таблицы вычислить величину дзета-потенциала указанного золя.
63–66. Каковы условия получения коллоидных растворов? Укажите вещества, которые могут служить стабилизаторами для указанных в таблице коллоидных систем, полученных в результате обменных реакций. Последнее изменение этой страницы: 2017-04-12; Просмотров: 1695; Нарушение авторского права страницы 💥 ВидеоКонформации молекулСкачать  Дипольный момент (видео 26) | Химические связи и структура молекул | ХимияСкачать  Популярная физическая химия для винокуров. Вторая беседа.Скачать  Перегонка|Краткий курс. Часть 4|Макаров С.Ю. (мак210)|винокурение|азбука винокураСкачать  НДРФ|Спирт этиловый недоректификат|РектификацияСкачать  Опыты по химии. Получение сложного эфираСкачать  Изоамиловый спирт ч.3. Вторая (дробная) перегонка с отбором изоамилового спиртаСкачать  Урок 197. Поверхностная энергия. Коэффициент поверхностного натяженияСкачать  В чём различие этилового и метилового спирта?Скачать  5.1. Адсорбция. Классификация адсорбцииСкачать  Горение спиртовСкачать  Установление эмпирической и молек. формул по массовым долям элем., входящих в состав в-ва. 10 класс.Скачать  5.2. Молекулярная адсорбция ПАВ на поверхности раздела раствор-воздухСкачать  5. Взаимодействие молекулСкачать  |




